|
CONTENTS
1. ьЄэь ыЊЉ
2. ьЄэыЊЉь
3. ьЄэы ьЇ
4. ьЄэьДыЁ
5. ьЄэыАЉыВ
6. ъИАъЕЌ ыА ььН
7. ьАИъГ ыЌИэ
R
REPORT
Preparation of CuCI
ъГМыЊЉыЊ
ьЇыъЕь
эъГМ
эыВ
ьДыІ
ь ьЖьМ
1. ьЄэь ыЊЉ: Preparation of CuCl
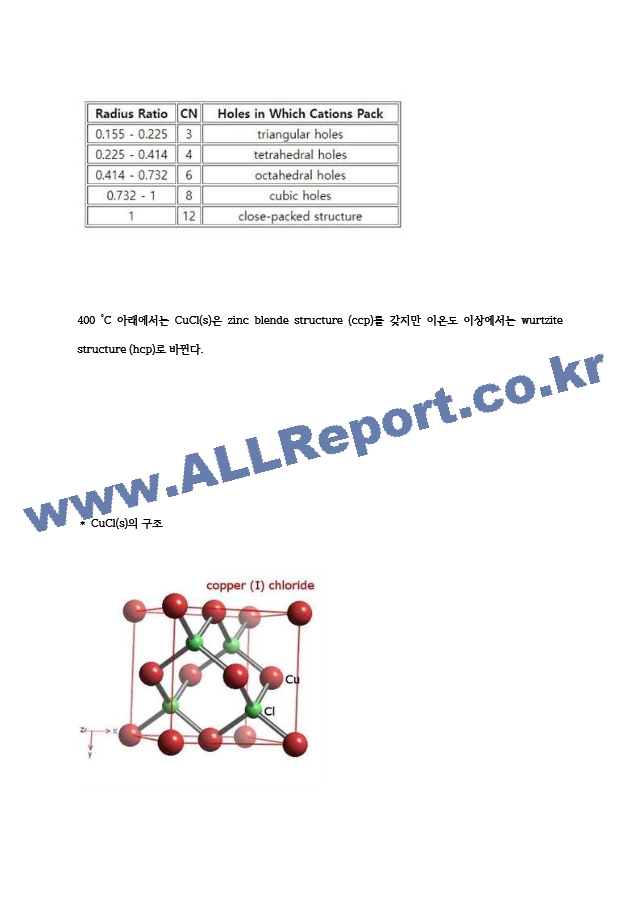
2. ьЄэыЊЉь : Cu(I) ь Cu(II) ьДьЈь ьь ы ыЙъЕыЅМ эЕэД ь CuCl(т
)ьД эьБыыьЇ ьъГ , CuCl2(т
Ё)ыЅМ эьььМ CuCl(т
)ыЅМ ь ьЁАэыЄ.
3. ьЄэы ьЇ: 22. 09. 30
4. ьЄэьДыЁ
ьЄэь ъДэД ьДэДэъИА ьэДьы Cu(I) ыА Cu(II) ьДьЈь ьыь ьИ ьь ьБъГМ Cu+ыЅМ ььБэы ъГМь , CuCl(s)ъА эьБыыЉД ьь эДьЇы ьДь ь ыэД ьььМ э эьъА ьыЄ. ы ьД ьЄэь ь ьээъИА ьэД эЙэ ьЄьэ, ььБыЌМь ь ыЖыІЌэДьМ эы ьДь ь ыэД ььыГМ ъВьДыЄ.
ъЕЌыІЌы ььь ь ьыААьЙьь ъАьЅ ыАъЙЅыЖыЖь dъЛьЇьД ыЖьь э ььДьЈь ыЇыы ььыЁ, ь ьДъИььДыЄ. Cu(I), Cu(II) ыА Cu(III)ыЁ ьЁДьЌэ ь ьыыА ъАьЅ ээ ъВь Cu(I)ь Cu(II)ьДыЄ. ъА ьАэ ьэьь stabilityы ыІЌъАыь ььДьЈ, ъЗИыІЌъГ ьЉыЇЄь эЙьБь ыАыМ ыЌыМьЇыЄ. ыГДэЕь ьДьЈ ээЉыЌМьь Cuы ьАэьъА +2ьИ ьАэьэ(3d9)ьДыЄ. Cu2+(aq) ьДьЈь ыАь эыьь ыэыДыыА, H2OъА ьы ыЄыЅИ ыІЌъАыь ьАЉыЌМь эьБэъВ ыыЉД ьъЙьД ыЌыМьЇ ь ьыЄ. ььЉьЁьь ьъЙь ыЄыЄы ъВь 3d ьЄыЙэьД ыЊЈы ьБььЇьЇ ььыЄы ъВь ьыЏИэыЄ. CuъА +1 ьАэьэъА ыыЉД 3d10 ъА ыъГ 3d ьЄыЙэьД ьь э ьБьь И ыЌДььД ыыЄ.
Cu+ъА ьъЙь ы ьЇ тІ(ьыЕ)
|